 |
|
| Appunti scientifiche |
|
 |
|
| Appunti scientifiche |
|
| Visite: 4199 | Gradito: |
Leggi anche appunti:Isomeria costituzionaleIsomeria costituzionale L'isomeria costituzionale o strutturale può essere Calcolo del pH di acidi e basi deboli molto diluiti e/o molto deboliCalcolo del pH di acidi e basi deboli molto diluiti e/o molto deboli Quando La mole ed il Peso molareLa mole ed il Peso molare Un concetto strettamente correlato al peso relativo |
 |
 |
Consideriamo ad esempio il seguente processo spontaneo di ossidoriduzione
Zn + Cu2+ → Zn2+ + Cu
dove lo zinco metallico si ossida in ione zinco perdendo due elettroni secondo la seguente semireazione
ossidazione Zn → Zn2+ + 2e-
e lo ione rame si riduce a rame metallico acquistando due elettroni secondo la seguente semireazione
riduzione Cu2+ + 2e- → Cu
Se vogliamo costruire una pila che si basi su tale reazione è necessario separare le due semireazioni. In ciascuna semicella dovrà dunque essere posto uno dei due metalli in equilibrio con il proprio catione.
Una pila che utilizza proprio la reazione di ossidoriduzione tra rame e zinco è la pila Daniell.
Le specie chimiche che partecipano alla reazione redox in ciascuna semicella sono dette coppie redox.
Ciascuna coppia redox viene sempre convenzionalmente scritta nel senso della reazione di riduzione, prima la specie ossidata (ox) e poi la specie ridotta (red) separate da una barra diagonale (ox/red)
Le coppie redox utilizzate nella pila Daniell, scritte dunque nel senso della reazione di riduzione, sono
Cu2+/ Cu e Zn2+/ Zn
Nella pila Daniell una barretta di zinco metallico viene immersa in una soluzione di solfato di zinco che, dissociandosi completamente, fornisce gli ioni Zn2+, mentre una barretta di rame metallico viene immersa in una soluzione di solfato rameico che fornisce gli ioni Cu2+.
In questo caso particolare le due barrette metalliche fungono anche da elettrodi (o collettori di elettricità), cioè da supporto per il passaggio degli elettroni da una semicella all'altra quando avviene la reazione. In altre pile, dove le specie chimiche che reagiscono non sono conduttrici, è necessario utilizzare elettrodi inerti (che non partecipano alla reazione) per consentire agli elettroni di muoversi.
Si tenga tuttavia presente che il termine elettrodo viene comunemente utilizzato per indicare anche l'intera semicella.
In definitiva un elettrodo è
in senso lato l'intera semicella (o semielemento)
in senso stretto la parte conduttrice della semicella che estrae o immette corrente elettrica nella semicella.
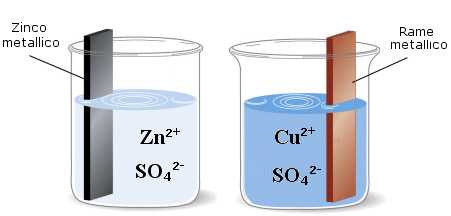
Finché le due semicelle rimangono separate non si osserva naturalmente alcuna reazione. Ma se colleghiamo con un filo metallico i due elettrodi, lo Zinco, che ha una maggiore tendenza ad ossidarsi rispetto al Rame, perde elettroni. Gli elettroni, passando attraverso il conduttore metallico, vengono attirati dagli ioni rameici che li acquistano e si riducono.
In tal modo dello zinco metallico si ossida e passa in soluzione sotto forma di ione Zn2+ (lo ione zinco è solubile). La soluzione di solfato di zinco si arricchisce di ioni Zn2+ mentre l'elettrodo di Zinco si assottiglia.
Nell'altra semicella invece gli ioni rameici a contatto con l'elettrodo si riducono a rame metallico aderendo all'elettrodo stesso. La soluzione si impoverisce di ioni Cu2+ mentre l'elettrodo aumenta la sua massa.
Convenzionalmente:
l'elettrodo al quale avviene la reazione di ossidazione è detto Anodo
l'elettrodo al quale avviene la reazione di riduzione è detto Catodo.
Poiché, quando in una pila colleghiamo gli elettrodi chiudendo il circuito, gli elettroni si muovono dall'anodo al catodo, l'anodo risulta essere l'elettrodo negativo (essendo la sorgente delle cariche negative, gli elettroni), mentre il catodo è l'elettrodo positivo.
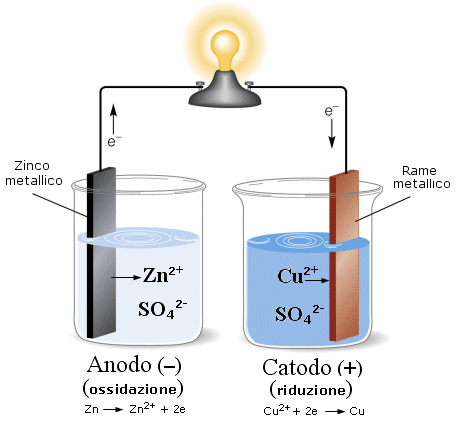
Mentre la reazione procede la soluzione di solfato di zinco tende ad arricchirsi di ioni positivi (Zn2+) e la soluzione di solfato rameico tende ad impoverirsi di ioni positivi (Cu2+). A causa di ciò le due semicelle perdono la loro elettroneutralità.
La semicella anodica tende a caricarsi positivamente [Zn2+] > [SO42--], mentre la semicella catodica tende a caricarsi negativamente [Cu2+] < [SO42-].
In queste condizioni il passaggio di corrente elettrica si esaurirebbe ben presto, in quanto gli elettroni (negativi) dovrebbero allontanarsi da una soluzione positiva, che li attrae, per andare verso una soluzione negativa, che li respinge.
La perdita progressiva dell'elettroneutralità da parte delle due semicelle diventa perciò responsabile di un potenziale elettrico che agisce in senso contrario a quello originario. Quando l'intensità dei due potenziali assume lo stesso valore assoluto, la corrente cessa.
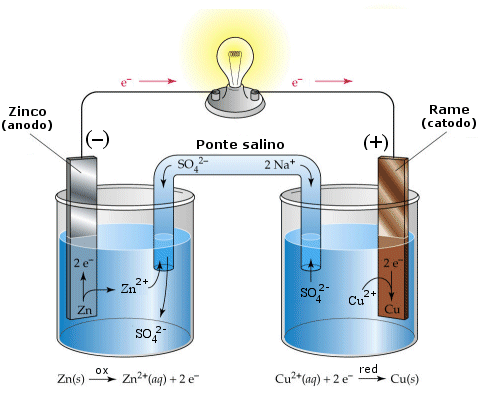
Per ovviare a tale inconveniente è quindi necessario garantire l'elettroneutralità delle due soluzioni. Per questo motivo le soluzioni vengono collegate con un dispositivo, detto ponte salino, che fornisce loro ioni di segno opposto.
Un esempio di ponte salino potrebbe essere un tubo contenente una soluzione molto concentrata di un elettrolita forte (ad esempio un sale), i cui ioni non interferiscano chimicamente con le reazioni in corso. Le due estremità del tubo vengono immerse nelle semicelle ed occluse con materiale filtrante (ovatta) in modo che gli ioni di carica opposta possano diffondere lentamente.
Se ad esempio utilizziamo un generico sale BA, in grado di dissociarsi in ioni B+ e A-, gli ioni B+ diffonderanno nella soluzione catodica, mentre gli ioni A- in quella anodica, garantendo l'elettroneutralità.
Il ponte salino può essere sostituito da un setto poroso che divida le due soluzioni (ad esempio porcellana non verniciata) e permetta all'eccesso relativo di ioni SO42- di diffondere verso la soluzione positiva, impedendo agli ioni positivi di migrare.

Si noti infine che, se le due semicelle non venissero separate, i reagenti (Zn + Cu2+) verrebbero a contatto all'interno della soluzione e gli elettroni, invece di circolare all'esterno della pila, produrrebbero un corto circuito interno.
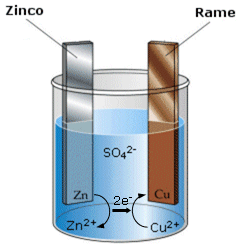
corto circuito
Esistono tuttavia pile in cui i reagenti sono presenti in fasi separate e non a contatto tra di loro. In tali pile le semicelle sono unite in un unico sistema e possono quindi non necessitare di ponti salini.
 |
| Appunti su: https:wwwappuntimaniacomscientifichechimicala-pila-daniell93php, pila daniell molaritC3A0 soluzioni, pila daniell E pila carbone zinco, |
|
| Appunti Ingegneria tecnico |  |
| Tesine Geografia |  |
| Lezioni Biologia |  |