 |
|
| Appunti scientifiche |
|
 |
|
| Appunti scientifiche |
|
| Visite: 9410 | Gradito: |
Leggi anche appunti:I legami chimiciI legami chimici Obiettivi: verificare l'esistenza del legame ionico, Relazione tra ΔG° e E°Relazione tra ΔG° e E° La relazione esistente tra DG° e la costante IdrogenoIDROGENO Chimica 2 Idrogeno L'idrogeno era conosciuto sotto il |
 |
 |
Per il calcolo del pH di soluzioni di acidi e basi deboli non è sufficiente conoscere la loro concentrazione iniziale, in quanto gli acidi deboli non sono completamente dissociati in soluzione acquosa. Per determinare che concentrazione assumeranno gli ioni H+ (o OH-) è quindi necessario conoscere anche il valore della costante dell'equilibrio di dissociazione o costante di dissociazione.
Per un generico acido monoprotico HA, l'equilibrio di dissociazione è
HA ![]() H+ + A-
H+ + A-
La costante di equilibrio, nota come costante di dissociazione acida (o kappa acida) ka, vale
![]()
In analogia con la definizione di pH, anche per la costante di dissociazione acida si utilizza il pka.
pka = - log10 (ka)
Per gli acidi deboli poliprotici vi sono naturalmente tante costanti di
dissociazione quanti sono gli atomi di idrogeno dissociabili (costante di prima
dissociazione ![]() , costante di seconda dissociazione
, costante di seconda dissociazione ![]() , etc)
, etc)
Ad esempio per l'acido solforoso a 25°C si ha
H2SO3 ![]() H+ + HSO3-
H+ + HSO3- 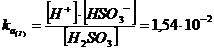
HSO3- ![]() H+ + SO32-
H+ + SO32- 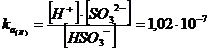
Naturalmente l'acido cede più facilmente il primo ione H+, mentre il secondo ione H+, che deve abbandonare uno ione negativo ed è quindi trattenuto con maggior forza, si separa con maggior difficoltà.
A conferma di quanto detto si può notare come nell'esempio riportato il
valore di ![]() sia molto minore
del valore di
sia molto minore
del valore di ![]() . Il primo equilibrio di dissociazione è quindi più
spostato verso destra del secondo.
. Il primo equilibrio di dissociazione è quindi più
spostato verso destra del secondo.
Si tratta di un comportamento generale. Tutti gli acidi deboli poliprotici presentano infatti valori decrescenti per le costanti di dissociazione successive alla prima.
Quanto detto per gli acidi deboli vale anche per le basi deboli. Ad esempio per una generica base BOH, l'equilibrio di dissociazione è
BOH ![]() B+ + OH -
B+ + OH -
La costante di equilibrio, nota come costante di dissociazione basica (o kappa basica) kb, vale
![]()
Naturalmente anche per le basi deboli vi possono essere tante kb quanti sono i gruppi ossidrili dissociabili. Ovviamente, anche la costante di dissociazione basica può essere espressa come pkb.
pkb = - log10 (kb)
Il valore assunto dalla costante di dissociazione è utilizzato come una misura della forza di un acido (o di una base), in quanto è indipendente dalla concentrazione iniziale dell'elettrolita. Possiamo in altre parole affermare che un acido (o una base) è tanto più debole quanto più basso è il valore della sua costante di dissociazione.
Ad esempio l'acido ipocloroso, HClO (ka = 2,95.10-8) è più debole dell'acido fluoridrico HF (ka = 3,53.10-4).
Il grado di dissociazione di un acido (o di una base) non può essere usato come misura della sua forza in quanto si può facilmente dimostrare che esso varia con la concentrazione iniziale.
Sia ad esempio HA un acido debole generico, ka la sua costante di dissociazione e Ciniz la sua concentrazione iniziale. Se è il suo grado di dissociazione, all'equilibrio si formeranno aCiniz mol/l di ioni H+ e aCiniz mol/l di ioni A-, mentre rimarranno indissociate (Ciniz - aCiniz ) mol/L di HA.
Riportiamo quanto detto in una tabella
|
Specie |
Concentrazioni iniziali |
Concentrazioni all'equilibrio |
|
HA |
Ciniz |
Ciniz - α Ciniz |
|
H+ |
|
α Ciniz |
|
A- |
|
α Ciniz |
Se riportiamo ora i valori di equilibrio in funzione di ka, otteniamo
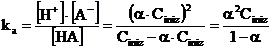
Da tale relazione (legge di diluizione di Ostwald) si deduce facilmente che, essendo ka costante, al diminuire della concentrazione iniziale il grado di dissociazione deve aumentare. In altre parole anche un acido debole, se molto diluito, può essere quasi completamente dissociato. Tutti gli elettroliti tendono a dissociarsi completamente quando la concentrazione tende a zero.
Naturalmente il fatto che un acido debole a concentrazioni molto basse sia molto dissociato non significa che in tali condizioni diventi forte. Infatti a basse concentrazioni dell'acido anche gli ioni H+ che si producono sono complessivamente molto pochi ed il pH rimane sempre molto vicino a 7.
Calcoliamo ad esempio il pH ed il grado di dissociazione di una soluzione 1M e di una soluzione 10-2 M di acido fluoridrico (ka = 3,53.10-4).
L'acido fluoridrico è un acido debole e si dissocia secondo il seguente equilibrio
HF ![]() H+ + F -
H+ + F -
Se poniamo pari ad x il numero di mol/l di HF che si dissociano, possiamo costruire la seguente tabella delle concentrazioni iniziali e delle concentrazioni di equilibrio
|
Specie |
Concentrazioni iniziali |
Concentrazioni all'equilibrio |
|
HF |
|
1 - x |
|
H+ |
|
x |
|
F- |
|
x |
Poniamo ora le concentrazioni di equilibrio, espresse in funzione di x, in relazione con la ka
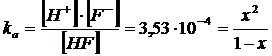
Risolvendo rispetto ad x si ottiene
[H+] = x = 1,86.10-2 mol/l
il pH vale
pH = -log [H+] = -log 1,86.10-2 = 1,73
mentre il grado di dissociazione risulta pari a
![]()
Risultano quindi dissociate quasi 2 molecole ogni 100.
Vediamo ora come varia il pH ed il grado di dissociazione diluendo la soluzione.
Se la concentrazione iniziale della soluzione è ora pari a 10-2 mol/L, la relazione di equilibrio diventa

Risolvendo rispetto ad x si ottiene
[H+] = x = 1,71.10-3 mol/l
il pH vale
pH = -log [H+] = -log 1,71.10-3 = 2,77
mentre il grado di dissociazione risulta pari a
![]()
Risultano quindi dissociate quasi 2 molecole ogni 10.
Diminuendo la concentrazione iniziale è dunque aumentata la percentuale di molecole che si dissociano. Nonostante questo il pH è aumentato, a dimostrazione del fatto che la seconda soluzione è meno acida della prima.
In generale per calcolare il grado di dissociazione è necessario risolvere la seguente equazione di secondo grado, che si ottiene riordinando la relazione di Ostwald
![]()
dove si osserva che il grado di dissociazione dipende dal rapporto tra la concentrazione iniziale dell'acido e la sua costante di dissociazione. Riportiamo a titolo di esempio alcuni valori del grado di dissociazione in funzione del rapporto C/ka.
|
C/ka |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Si noti che se C/ka > 102 il grado di dissociazione è inferiore al 10%. In questa condizione la quantità di acido che si dissocia può essere consideratata trascurabile rispetto alla quantità di acido iniziale.
Inoltre, poichè per C/ka > 102 il grado di dissociazione α è molto inferiore all'unità, si avrà che (1 - α) ≈ 1 e la relazione di Ostwald può essere approssimata nel modo seguente
![]()
Se ne deduce che, per C/ka > 102 il grado di dissociazione α può essere stimato con la seguente relazione approssimata
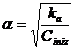
 |
| Appunti su: https:wwwappuntimaniacomscientifichechimicaph-in-soluzioni-di-acidi-e-bas83php, pka e pkb, pkb chimica, relazione ka e pka, pka e pkb chimica, |
|
| Appunti Ingegneria tecnico |  |
| Tesine Geografia |  |
| Lezioni Biologia |  |