 |
|
| Appunti scientifiche |
|
 |
|
| Appunti scientifiche |
|
| Visite: 4787 | Gradito: |
Leggi anche appunti:Confronto conducibilità misurata e calcolataConfronto conducibilità misurata e calcolata Per quanto riguarda il confronto La 5'-nucleotidasi citosolica II (cN-II)La 5'-nucleotidasi citosolica II (cN-II) 1 Distribuzione tissutale La Equilibrio di solubilità e precipitazioneEquilibrio di solubilità e precipitazione La conoscenza del valore del prodotto |
 |
 |
Le mutazioni sono alterazioni casuali, permanenti ed ereditarie dell'informazione genetica di una cellula a livello della struttura o dell'organizzazione del suo DNA.
Il DNA è suscettibile di danneggiamento
Essendo modificazioni casuali a carico di un'informazione altamente strutturata ed ordinata, le mutazioni hanno una bassissima probabilità di produrre una alterazione favorevole dell'organismo. È un po' come se dessimo in mano i circuiti di un televisore ad una scimmia. La probabilità che alla fine riesca a trasformarli in quelli di un computer è praticamente nulla.
La maggior parte delle mutazioni sono dunque eventi sfavorevoli per l'individuo in cui si manifestano. Alcune di esse possono essere anche cancerogene (o teratogene), trasformando la cellula che le subisce in una cellula tumorale. In alcuni casi possono essere addirittura letali. Si deve comunque tener presente che le conseguenze per un organismo di una mutazione dannosa sono diverse a seconda che si manifestino a carico delle cellule somatiche o delle cellule germinali (riproduttive).
Se una cellula mutata dà origine solo a cellule somatiche (non sessuali) verrà prodotta un'area o un settore mutato ma queste nuove caratteristiche non verranno trasmesse alle generazioni successive. Questo tipo di mutazione è chiamata mutazione somatica.
Se, al contrario, la mutazione avviene nella linea germinale (cellule sessuali
o riproduttive) di organismi che si riproducono sessualmente, la mutazione potrà
essere trasmessa alla generazione successiva dando origine ad un individuo
mutato sia nelle sue cellule somatiche sia nella linea germinale. Queste mutazioni vengono chiamate mutazioni della linea germinale.
Tuttavia, in una prospettiva biologica più ampia rispetto a quella del singolo individuo, le mutazioni sono considerate un evento fondamentale e positivo per l'evoluzione biologica. Le mutazioni sono infatti le principali responsabili della comparsa di nuovi geni e di nuovi alleli. In questo modo le mutazioni creano nuova variabilità genetica sulla quale può agire la selezione naturale. In assenza di mutazioni una specie non potrebbe evolvere ed avrebbe una elevata probabilità di non adattarsi alle modificazioni ambientali e conseguentemente di estinguersi.
Il valore biologico delle mutazioni non è dunque univoco: è in genere negativo per il singolo individuo, mentre è positivo per la specie (dal che si deduce che gli interessi del singolo individuo non coincidono necessariamente con gli interessi della specie alla quale appartiene).
Gli agenti mutageni fisici sono il calore, le radiazioni elettromagnetiche ad alta energia (raggi UV, raggi X e raggi gamma) e le radiazioni corpuscolari (radiazione alfa (nuclei di elio), radiazione beta (elettroni), neutroni e protoni). I mutageni fisici degradano il DNA, spezzandone i legami chimici.
Gli agenti mutageni chimici si classificano in analoghi dei nucleotidi, modificatori ed intercalanti.
Gli analoghi dei nucleotidi (o analoghi delle basi) sono molecole che presentano una somiglianza chimica con le normali base azotate, ma che la cellula non riconosce come diverse ed incorpora nel nuovo DNA che sintetizza.
Gli agenti modificatori (alchilanti, idrossilanti, deaminanti) alterano la struttura molecolare delle basi causando appaiamenti errati
Gli agenti intercalanti (acridine, bromuro di etidio) si inseriscono fra le basi azotate, legandosi ad esse e causano inserzioni e delezioni durante la replicazione del DNA.
Le mutazioni genetiche si classificano in geniche, cromosomiche e genomiche.
Le mutazioni geniche alterano un singolo gene, modificando una singola base azotata. Poiché avvengono in un punto preciso del gene sono anche dette mutazioni puntiformi.
Si classificano in mutazioni geniche per sostituzione, inserzione e delezione.
Le mutazioni geniche per sostituzione producono la sostituzione di una base azotata (ed ovviamente anche della sua complementare), modificando una tripletta di basi che codifica per un amminoacido. Gli effetti possono essere diversi. Infatti la nuova tripletta potrà codificare per il medesimo amminoacido, per nessun amminoacido o per un amminoacido diverso.
Nel caso la nuova tripletta codifichi per il medesimo amminoacido (sappiamo che più triplette possono codificare per il medesimo amminoacido), la sostituzione non avrà alcun effetto sulla struttura primaria della proteina (sequenza degli amminoacidi) e la mutazione si definisce mutazione silente.
Nel caso la nuova tripletta non codifichi per nessun amminoacido (tripletta STOP), la proteina mutata si spezza in due frammenti e perde ovviamente la sua funzionalità. La mutazione è definita mutazione non-senso.
Nel caso la nuova tripletta codifichi per un amminoacido diverso la sostituzione viene definita mutazione di senso (missense) ed i suoi effetti sulla funzionalità proteica dipendono dal punto in cui è avvenuta la mutazione. In una proteina possiamo infatti individuare dei tratti funzionali, la cui alterazione comprometterebbe l'attività della molecola, e dei tratti non funzionali in cui la sostituzione di un amminoacido non produce effetti.
Le sostituzioni amminoacidiche in tratti funzionali possono dunque alterare in modo più o meno grave la funzionalità proteica. Ne è un esempio l'anemia falciforme, una malattia genetica recessiva, in cui i globuli rossi assumono una caratteristica forma a falce. L'anemia falciforme è dovuta alla sostituzione di un unico amminoacido (valina al posto dell'acido glutammico) nelle catene beta dell'emoglobina.
Le sostituzioni amminoacidiche in tratti non funzionali sono dette mutazioni neutre. Tali mutazioni non portano infatti ne' vantaggi ne' svantaggi, poiché lasciano inalterata la funzionalità proteica. Per questo motivo le mutazioni neutre non sono "viste" dalla selezione naturale e possono pertanto accumularsi con ritmo costante ed in punti casuali all'interno delle regioni non funzionali di una proteina.
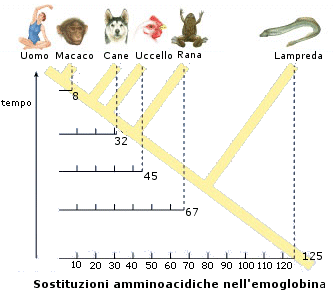
Le mutazioni neutre sono alla base degli orologi molecolari che i biologi utilizzano per ricostruire gli alberi filogenetici dell'evoluzione.
Un orologio molecolare è una proteina che si trova in molte specie diverse (proteina ubiquitaria), ad esempio l'emoglobina nei mammiferi o il citocromo c utilizzato nella catena respiratoria. Confrontando dunque la struttura primaria di una medesima proteina che si trova in due specie differenti (ad esempio l'emoglobina del cavallo con quella del cane) si possono evidenziare il numero di mutazioni neutre accumulatesi in termini di amminoacidi sostituiti. Una volta tarato l'orologio molecolare (cioè una volta stimato il tempo medio in milioni di anni affinché si accumuli una mutazione neutra), è possibile trasformare il numero di mutazioni trovate nel tempo trascorso dal momento in cui viveva l'antenato comune delle due specie studiate.
Le mutazioni geniche per inserzione provocano l'inserimento di un nuovo nucleotide.
Le mutazioni geniche per delezione provocano l'eliminazione di un nucleotide.
Queste mutazioni provocano oltre ad una modificazione del significato della tripletta di nucleotidi mutata, anche una sfasatura nella lettura di tutte le triplette successive. Queste mutazioni sono note come mutazioni con slittamento del modulo di lettura (frame-shift). Il cambiamento di tutti gli amminoacidi successivi al punto in cui è avvenuta la mutazioni porta per lo più alla perdita della funzionalità proteica.

Le mutazioni cromosomiche (o aberrazioni) sono alterazioni della struttura dei cromosomi che interessano uno o più geni e che si producono per lo più come conseguenza di errori durante il crossing-over, tramite rotture ed errate ricomposizioni dei cromosomi. In genere, i cromosomi rotti tendono a ricomporre le rotture e a ripristinare le strutture originarie, ma a volte, può capitare che il processo di riparazione non risulti corretto e si originano cromosomi anomali con strutture nuove. Si possono, così, verificare perdite, duplicazioni, inversioni o trasferimenti di pezzi più o meno estesi di cromosoma. I geni si vengono così a trovare in una posizione diversa da quella originale. Dato che la regolazione dell'attività di un gene dipende, in parte, anche dalla sua localizzazione nel genoma, le mutazioni cromosomiche hanno, generalmente, effetti estremamente drammatici.
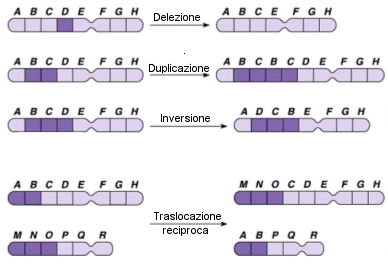
Le mutazioni cromosomiche si classificano in inversioni, traslocazioni, duplicazioni e delezioni.
L'inversione è una aberrazione strutturale cromosomica (riarrangiamento di struttura) che origina da due rotture sul cromosoma, successiva rotazione di 180° del tratto compreso tra le rotture e sua reintegrazione nel cromosoma stesso. Le inversioni possono essere pericentromeriche (comprendono la regione del centromero e le rotture si verificano sul braccio corto e sul braccio lungo del cromosoma) e paracentromeriche (non comprendono la regione del centromero e le due rotture si verificano sullo stesso braccio cromosomico). L'inversione si origina in genere durante l'appaiamento meiotico degli omologhi con formazione di un'ansa di inversione (loop).

La traslocazione (trasposizione) è una aberrazione cromosomica strutturale che consiste nel trasferimento di un segmento di cromosoma in una posizione errata, con un cambiamento nella localizzazione di un segmento cromosomico.
La traslocazione può essere intracromosomica o intercromosomica.
La prima implica un cambiamento di posizione
di un tratto cromosomico entro lo stesso cromosoma, sia da un braccio
cromosomico all'altro sia entro lo stesso braccio.
La seconda implica lo spostamento di un segmento cromosomico ad un altro non
omologo.
La traslocazione intercromosomica si definisce reciproca se ciascuno dei due cromosomi non omologhi trasferisce all'altro un proprio segmento.
La traslocazione intercromosomica si definisce non reciproca se il trasferimento è unidirezionale e solo uno dei due cromosomi trasferisce all'altro un proprio segmento.
Una traslocazione non reciproca tra cromosomi omologhi produce una delezione su di un cromosoma (quello che perde il segmento) ed una duplicazione sull'altro cromosoma (quello che riceve il segmento).
Le traslocazioni bilanciate sono il caso più fortunato: consistono infatti nello "scambio alla pari" di frammenti fra cromosomi diversi. Questo tipo di traslocazione non comporta perdita di materiale genetico e perciò i portatori di una traslocazione bilanciata non manifestano in genere alcun segno clinico. Nel caso di una traslocazione non bilanciata, uno o più cromosomi in seguito alla traslocazione hanno subito la perdita di materiale genetico, mentre altri ne hanno in sovrappiù. Chi è portatore di una traslocazione bilanciata, pur non manifestando alcun sintomo, rischia di avere figli portatori di traslocazioni patologiche (non bilanciate).
La delezione è una aberrazione cromosomica strutturale che porta alla perdita di un segmento di cromosoma. In alcuni casi è associata alla duplicazione, poiché il segmento reciso viene trasferito sul cromosoma omologo dove si trovano i medesimi alleli. In altri casi il segmento viene semplicemente perso. La delezione si produce in genere con una modalità analoga all'inversione, con formazione di un'ansa di delezione che, invece di risaldarsi in posizione invertita, si stacca.
Le delezioni si possono evidenziare in un cariotipo attraverso l'assenza di una o più bande cromosomiche, o addirittura di un intero braccio, come avviene ad esempio nella sindrome 18p (p indica il braccio corto di un cromosoma, q il braccio lungo), dove è avvenuta la completa delezione del braccio corto di uno dei due cromosomi 18. L'effetto di una delezione dipende dalla grandezza della porzione mancante e dal tipo di informazione genetica in essa contenuta: in una sola banda cromosomica possono trovarsi centinaia di geni. Le microdelezioni, rispetto alle delezioni, consistono nella perdita di frammenti cromosomici più piccoli e non sono evidenziabili attraverso un normale cariotipo.
La duplicazione è una aberrazione cromosomica strutturale che porta alla presenza di due segmenti genici identici all'interno di un medesimo cromosoma. La duplicazione è in genere sempre accompagnata dalla contemporanea delezione del segmento duplicato nel cromosoma omologo (il segmento viene infatti trasferito durante il crossing-over da un omologo all'altro).
Eventi mutazionali quali delezioni, inversioni o traslocazioni possono avvicinare o allontanare sequenze nucleotidiche precedentemente contigue e pertanto modificare anche drasticamente l'espressione di geni coinvolti in tali riarrangiamenti cromosomici. Il diverso tipo di espressione di un gene in funzione della posizione occupata dal gene stesso all'interno del cromosoma e dei rapporti con geni limitrofi è definito effetto di posizione.
|
Esempi di cariotipi anomali e loro interpretazione |
|
|
Cariotipo |
interpretazione |
|
47,XX,+21 |
Cariotipo femminile (XX) a 47 cromosomi (47), per la presenza di un cromosoma 21 sovrannumerario (+) (Sindrome di Down) |
|
47,XY,+21 |
Cariotipo maschile (XY) con cromosoma 21 sovrannumerario (+) |
|
45,X |
Cariotipo con monosomia del cromosoma X, solitamente associato alla sindrome di Turner |
|
47,XXX |
Cariotipo con trisomia del cromosoma X |
|
47,XXY |
Cariotipo con costituzione XXY dei cromosomi del sesso, associato alla sindrome di Klinefelter |
|
46,XY,t(1;3)(p32;q12) |
Cariotipo maschile in cui è presente una traslocazione (t) coinvolgente un cromosoma 1 ed un cromosoma 3. I punti di rottura della traslocazione sono localizzati a livello della banda 32 sul braccio corto (p) del cromosoma 1 ed a livello della banda 12 del braccio lungo (q) del cromosoma 3. |
|
46,XY, del(5p) |
Cariotipo maschile in cui è presente una delezione (del) del braccio corto (p) di un cromosoma 5. (Sindrome "cri-du-chat") |
|
46,XX, del(1)(p32.2) |
Cariotipo femminile in cui è presente una delezione (del) di parte del braccio corto (p) di un cromosoma 1, a livello della regione 3, nella banda 2, sottobanda 2. |
|
46,XY, inv(7)(p13;q22) |
Cariotipo maschile in cui è presente una inversione (inv) del cromosoma 7 del tratto che va dalla banda 13 del braccio corto (p) alla banda 22 del braccio lungo (q) |
|
46,XY, dup(2)(q11;q21) |
Cariotipo maschile in cui è presente una duplicazione (dup) del tratto che va dalla banda 11 alla banda 21 del braccio lungo (q) del cromosoma 2 |
Le mutazioni genomiche sono alterazioni del numero dei cromosomi, come conseguenza della perdita o dell'aggiunta di interi cromosomi (cromosomi soprannumerari). Le mutazioni genomiche sono per lo più causate da una mancata disgiunzione degli omologhi durante la meiosi. Durante la gametogenesi può infatti capitare che i cromosomi omologhi non si distribuiscano equamente nei gameti. Un gamete con una anomalia di questo tipo, con cromosomi in difetto o in eccesso rispetto al suo normale corredo aploide, fecondato da un gamete normale, darà luogo ad uno zigote che non presenterà il suo normale corredo diploide. Quando una cellula presenta il suo corredo cromosomico normale, aploide o multiplo di esso, si definisce euploide. La variazione della condizione euploide con variazione del numero corretto di cromosomi si definisce aneuploidia.
Le aneuploidie sono classificate da alcuni autori come aberrazioni cromosomiche.
La monosomia e la trisomia sono esempi di aneuploidia.
La monosomia è la presenza di un singolo cromosoma al posto di una coppia all'interno di un corredo diploide.
La trisomia è la presenza di tre omologhi al posto di una coppia all'interno di un corredo diploide.
Se la mancata disgiunzione riguarda l'intero corredo cromosomico si possono formare cellule polipoidi (triploidi 3n, tetraploidi 4n etc) con comparsa di intere serie di cromosomi soprannumerari. La poliploidia è in genere una condizione letale per gli animali, mentre nei vegetali è piuttosto diffusa (frumento, cotone, tabacco) e può produrre gigantismo e maggior produttività.

Il numero atipico di cromosomi può interessare sia i cromosomi sessuali che i restanti (autosomi) . Le anomalie degli autosomi comportano effetti fenotipici molto più gravi rispetto a quelli riconducibili ai cromosomi sessuali. La maggior parte dei feti con gravi anomalie degli autosomi non arriva alla nascita in quanto il loro sviluppo è talmente anormale che la gravidanza si risolve precocemente con aborto spontaneo. Nell'ambito delle anomalie cromosomiche, molto comune fra gli aborti naturali è la poliploidia.
Aneuploidie autosomiche
Le anomalie degli autosomi, diversamente da quelle dei cromosomi sessuali, comportano effetti talmente gravi che sono compatibili con la vita solo la trisomia 21, responsabile della sindrome di Down, la trisomia 13, responsabile della sindrome di Patau e la trisomia 18, responsabile della sindrome di Edwards. Le altre trisomie complete non sono compatibili con la vita e quando sono presenti in un feto sono causa di aborto spontaneo.
La sindrome di Down o trisomia 21 è causata dalla mancata disgiunzione dei cromosomi della coppia 21 in tre copie. Le persone con tale sindrome hanno in tutte le loro cellule 47 cromosomi con il cromosoma 21. L'incidenza della trisomia aumenta drasticamente con l'età della madre. Gli affetti presentano palpebre anomali, naso schiacciato, lingua larga, mani corte e robuste, statura bassa, ritardo mentale, probabili malformazioni cardiache, attesa di vita minore del normale.
La sindrome di Patau o trisomia 13 è caratterizzata da gravi ritardi mentali. L'incidenza è più bassa rispetto alla sindrome di Down, ma come questa è legata all'età della madre. Gli affetti manifestano malformazioni fisiche come cranio ed occhi piccoli, e, molto spesso, difetti cardiaci, dita soprannumerarie e sordità.
La sindrome di Edwards o trisomia 18 è caratterizzata da ritardo mentale e fisico. Gli affetti manifestano cranio allungato, orecchie con basso punto di attacco, cavità orale piccola e difetti cardiaci.
Aneuploidie cromosomi sessuali
Le anomalie più frequenti dei cromosomi sessuali sono le trisomie XXX, XXY, XYY e la monosomia X0, dove 0 sta per assenza dell'omologo del cromosoma X. Essendo la Y mascolinizzante, la sua presenza indica il sesso maschile.
La trisomia XXY o sindrome di Klinefelter è causata dalla non disgiunzione delle X nella produzione dell'ovulo. Gli individui affetti sono maschi con testicoli non sviluppati, mancata produzione di spermatozoi, assenza di pelosità e barba, tono della voce che resta acuto. In genere, tali sintomi si accompagnano a statura alta e funzione intellettuale leggermente deficitaria.
La monosomia X0 o sindrome di Turner produce femmine di bassa statura, collo tozzo e corto, organi sessuali infantili, assenza spesso di ovaie. Le capacità intellettive, in genere, risultano quasi normali.
Gli affetti della trisomia XXX sono femmine quasi normali sul piano fisico e riproduttivo, ma manifestano, molto spesso, consistenti ritardi mentali.
Gli affetti della trisomia XYY sono maschi che, a parte la tendenza a superare mediamente i 180 cm di statura, non manifestano sintomi fisici particolari. La trisomia XYY, data l'alta frequenza riscontrata nelle carceri, fu sospettata, dopo gli anni 60, di essere una probabile causa di comportamenti violenti. Studi approfonditi, però, hanno fatto rientrare del tutto tali sospetti. La trisomia XXY è causata da una mancata disgiunzione dei due cromatidi che formano il cromosoma Y durante la seconda divisione meiotica.
 |
| Appunti su: Mutazioni Genetiche Riassunto, mutazione cromosomica, mutazioni frameshift, delezione duplicazione inversione traslocazione, delezione cromosomica, |
|
| Appunti Biologia |  |
| Tesine Geografia |  |
| Lezioni Ingegneria tecnico |  |